JACS│上海药物所发展光交联策略揭示Midnolin蛋白质互作组及非泛素依赖性降解底物
2026年3月12日,中国科学院上海药物研究所陈小华和谭敏佳团队在《美国化学会志》(Journal of the American Chemical Society )上发表了题为“Multiplexed Photo-Cross-Linking Reveals Comprehensive Midnolin Interactome: Insights into Ubiquitin-Independent Degradation and Functional Diversity”的研究论文。该研究创新性地发展了多重光交联化学生物学策略,系统解析了Midnolin的蛋白质互作组,深入揭示了其介导的非泛素依赖的底物降解机制,显著拓展了Midnolin的降解底物谱及潜在的可调控蛋白空间,为靶向“难成药”靶标的降解提供了新思路。
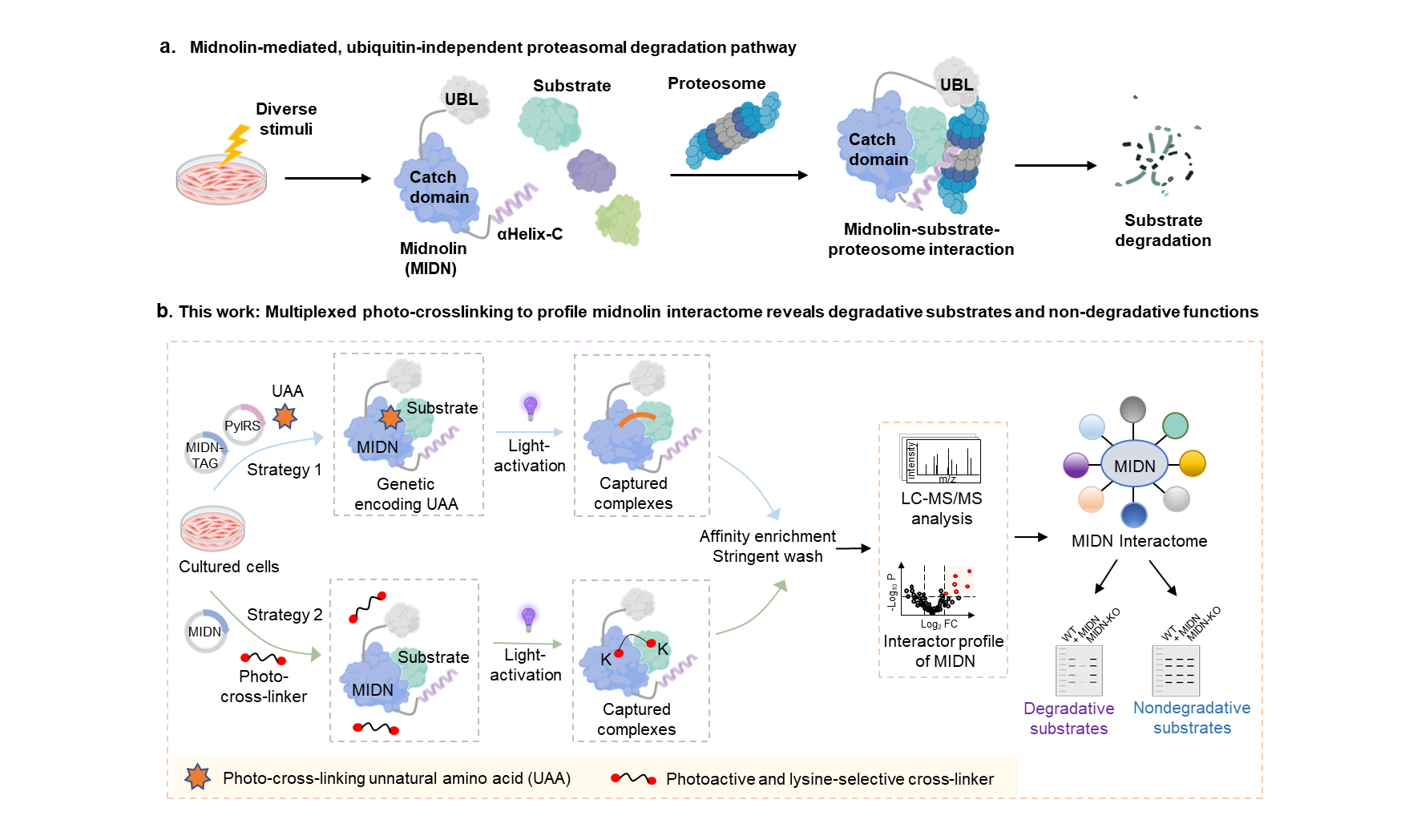
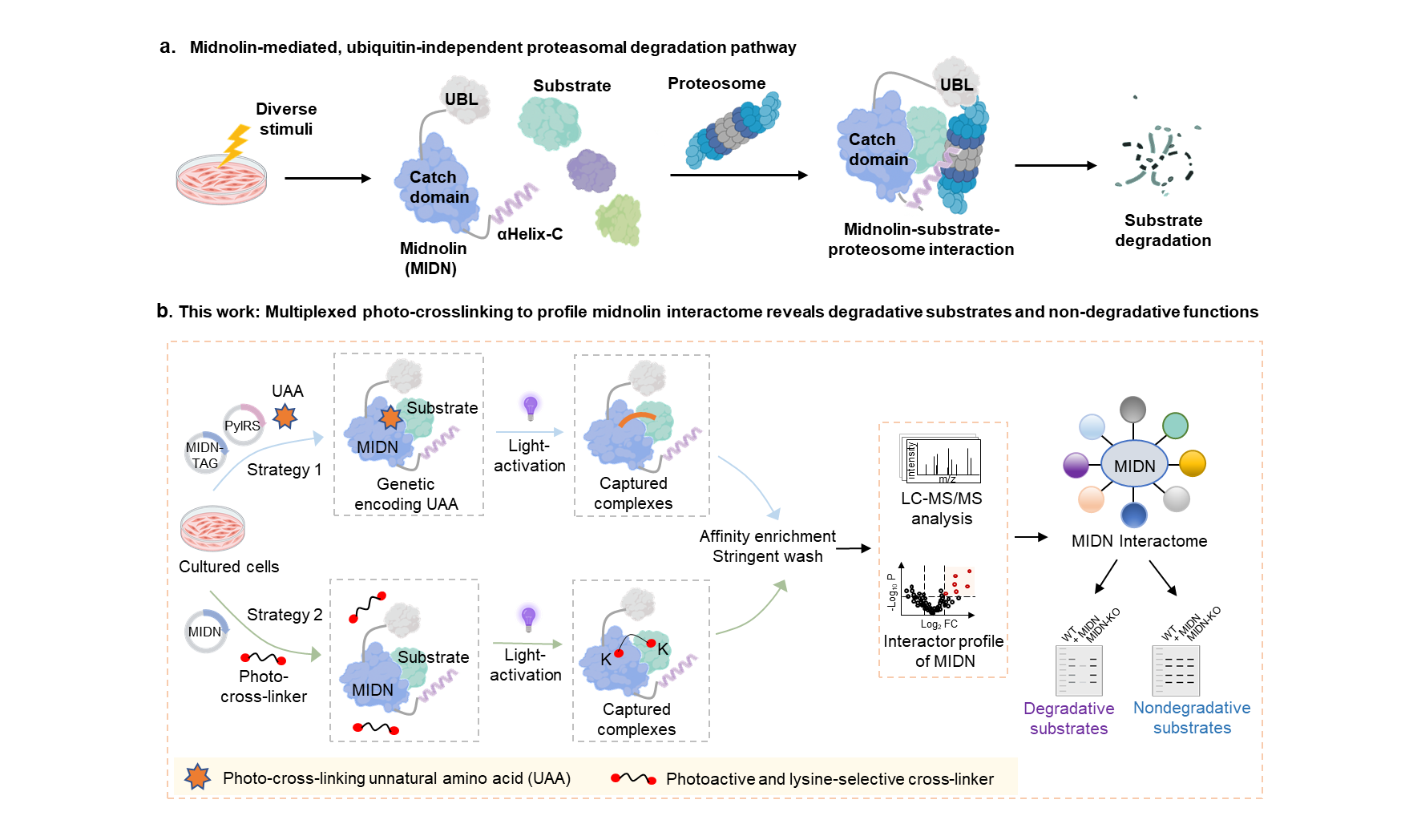
蛋白质降解是细胞维持蛋白稳态、调控关键生命活动的核心过程,泛素-蛋白酶体系统与溶酶体系统是细胞内主要的蛋白降解途径。近年来发现的Midnolin-蛋白酶体途径作为一种非泛素依赖性的蛋白降解机制,可绕过经典的泛素化过程,直接招募底物至蛋白酶体进行降解(图1a),展现靶向传统“难成药”靶标的巨大潜力。尽管Midnolin在多种癌症(如肝癌、乳腺癌、胃癌、多发性骨髓瘤)和神经退行性疾病(如帕金森病)中被报道扮演重要角色,但由于Midnolin与其互作蛋白之间往往是动态或微弱的相互作用,现有方法难以全面、精确地发现其完整的互作组(包括降解底物和非降解互作蛋白),极大地限制了对Midnolin功能多样性的理解及其治疗潜力的挖掘。
基于课题组前期发展的PANAC光点击化学生物学工具及蛋白质动态互作研究的基础(Chem, 2019, 5, 2955;Nat. Commun. 2020, 11, 5472; Nat. Chem. 2023, 15, 803,Nat. Commun. 2024, 15, 1465; Angew. Chem. Int. Ed. 2025, 64, e202507254;Angew. Chem. Int. Ed. 2025, 64, e202505053),本研究构建了一种高效的多重光交联平台 (图1b),一方面,采用具有赖氨酸选择性的光交联剂(如CO-cross-linker),实现对Midnolin互作蛋白的精准捕获;一方面,通过基因密码子扩展技术,可将具有光交联活性的非天然氨基酸(如AbK)定点引入到Midnolin的Catch结构域中,在光激活下实现活细胞内Midnolin与互作蛋白的共价捕获。该研究结合光交联技术和蛋白质组学分析,能高灵敏、有效地揭示Midnolin的蛋白质互作组。该研究成功鉴定一批Midnolin的互作蛋白,显著扩展了Midnolin已知的互作蛋白谱,为深入理解其细胞功能奠定了基础。研究首次发现并验证了4个新的Midnolin降解底物(ETV3、JUN、PRKD1和FN3KRP)。值得注意的是这些新底物是现有基于蛋白质稳定性的荧光筛选方法无法检测到的,凸显了本研究平台在发现Midnolin互作底物方面的独特优势。其中的研究结果揭示Midnolin能够介导转录因子JUN蛋白的非泛素依赖的蛋白酶体途径降解,提示通过Midnolin介导JUN降解在疾病治疗中的潜力。除了降解底物,研究中还发现了多个Midnolin的非降解互作蛋白,揭示了Midnolin在降解之外调控底物蛋白的其他细胞功能。
综上所述,本研究发展的多重光交联策略,不仅为解析Midnolin在不同生物学背景下的蛋白质互作提供了有效的化学生物学工具,而且为传统药物难以干预的致病蛋白(尤其是泛素-蛋白酶体途径难以降解的蛋白)的发现和降解提供了创新途径,并为开发新一代靶向蛋白降解策略提供新的思路。该研究有助于深入理解Midnolin在非泛素依赖的底物降解过程中的作用及其在细胞中的多方面功能,有望促进疾病治疗新靶标和干预策略的开发。
上海药物所副研究员许亚莉、同济大学博士后赵雯思和南京中医药大学硕士联培生傅晶晶为本论文的共同第一作者。上海药物所陈小华研究员和谭敏佳研究员为本论文的通讯作者。该工作得到国家自然科学基金和上海市浦江项目的支持。
原文链接:https://pubs.acs.org/doi/10.1021/jacs.5c22099
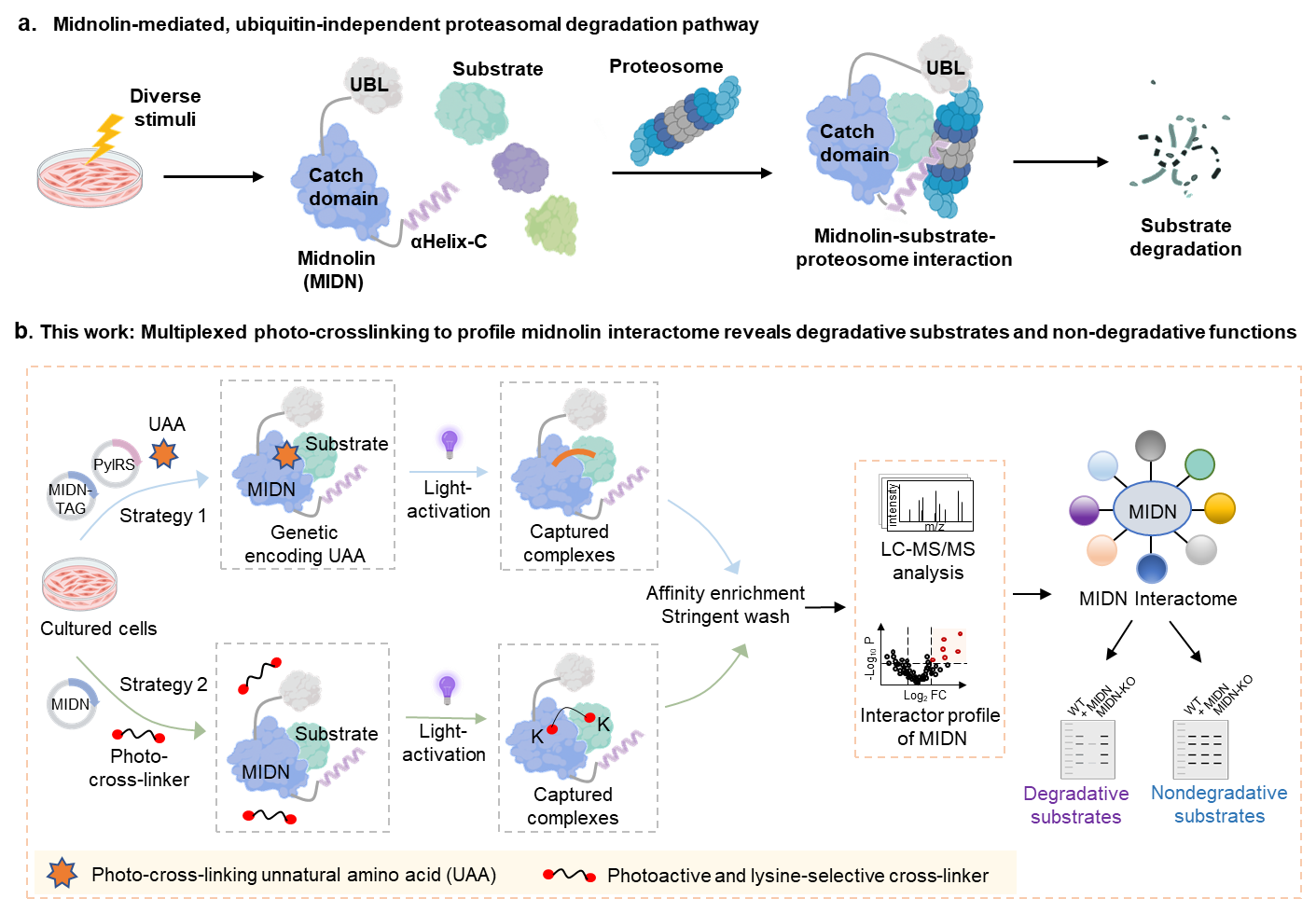
图1. 本工作发展的多重光交联化学生物学策略,揭示Midnolin蛋白质互作组及其介导的非泛素依赖降解底物
(供稿部门:陈小华课题组;供稿人:许亚莉)