Theranostics︱靶向Aβ蛋白的近红外荧光小分子探针的发现和成像研究
阿尔兹海默病(Alzheimer’s Disease,AD)是一种严重的神经退行性疾病,其起病隐匿,病程长,病因复杂,严重影响患者的生活质量,给患者家庭和社会带来巨大的经济负担。AD的主要病理特征之一表现为患者脑部出现β-淀粉样蛋白(β-Amyloid proteins,Aβ蛋白)的沉积。开发能特异性靶向Aβ蛋白,特别是AD早期的Aβ蛋白单体和寡聚体的分子影像探针,对于AD的早发现和早治疗,以及抗AD药物治疗效果的早期评估都具有重要意义。
2022年4月4日,中国科学院上海药物研究所柳红课题组与南京大学化学化工学院叶德举课题组合作构建了靶向Aβ蛋白的近红外荧光小分子探针,并应用于转基因AD模型小鼠脑部Aβ蛋白的实时荧光成像与可视化。该成果以 “Engineering of donor-acceptor-donor curcumin analogues as near-infrared fluorescent probes for in vivo imaging of amyloid-β species”为题发表于国际知名学术期刊Theranostics上。
近红外荧光成像由于具有灵敏度高、成像快捷、操作简便等优点,已被广泛应用于疾病标志物的检测中。近年来,研究人员也相继开发了Aβ蛋白响应的荧光探针用于Aβ蛋白的检测。但是,目前报道的荧光探针大多还存在荧光发射波长较短,与Aβ蛋白的结合动力学过程较慢、亲和力较低,以及仅能检测AD病程较晚期的Aβ蛋白斑块等不足。因此,发展具有近红外荧光发射波长,对Aβ蛋白单体、寡聚体和聚集体具有快速响应和高亲和力的近红外荧光探针用于活体内Aβ蛋白的高灵敏度和高特异性检测,对AD的早期诊断和疗效监测具有重要意义。
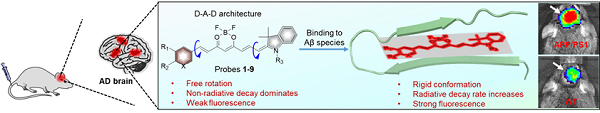
该工作基于Aβ单体、寡聚体和聚集体的蛋白结构与结合模式,通过理性设计和官能团替换,设计并合成得到9个具有Donor-Acceptor-Donor(D-A-D)结构的近红外荧光探针(1-9),可以与Aβ蛋白单体、寡聚体和聚集体高特异性结合并产生显著增强的近红外荧光信号。
该研究中发现的探针9具有较红的近红外荧光发射波长,较高的荧光量子产率,一方面可提高光对颅骨和头皮的穿透深度,从而提高探针活体上检测Aβ蛋白的灵敏度;另一方面可降低探针在活体应用时的给药剂量,从而减少了高剂量探针对神经系统的潜在毒性。此外,探针9因引入具有一定亲水性能的羟乙基官能团,改善了探针的理化性质,提高了探针的进脑量。同时,探针9表现出快速的结合动力学过程(< 120 s),较高的检测灵敏度和良好的选择性。在研究过程中,进一步利用正置荧光显微镜进行脑部微区实时动态荧光成像发现,探针9可快速穿透血脑屏障,进入脑实质,并与脑部的Aβ蛋白结合,产生“激活的”近红外荧光信号,以此有效区分转基因AD模型小鼠与对照野生型小鼠。
因此,探针9可高灵敏度、高特异性地检测Aβ蛋白单体、寡聚体和聚集体,并在活体上有效区分6月龄的早期AD模型小鼠与对照野生型小鼠,可用于AD的精确诊断,进而对AD进行早期发现和干预治疗。探针9有望作为一种检测Aβ蛋白的有效工具,并应用于实时评估抗AD药物的治疗效果。
沈阳药科大学与上海药物所的联合培养博士生房大庆、南京大学化学化工学院的文锡旦为该文章的共同第一作者。上海药物所柳红研究员、南京大学化学化工学院叶德举教授为该文章的共同通讯作者。该研究得到了国家自然科学基金、江苏省自然科学基金以及南京大学优秀研究项目的资助。
探针与Aβ蛋白响应机理示意图