ANGEW |上海药物所周兵/唐炜/许叶春团队设计“变构+竞争”双重作用模式的高选择性RIPK1抑制剂
细胞程序性坏死(Necroptosis)是一种受控的细胞坏死方式,受体相互作用激酶1(RIPK1)在死亡受体介导的细胞程序性坏死通路中发挥关键作用。越来越多的研究表明,开发靶向RIPK1的高活性、高选择性抑制剂能够为炎症性疾病、神经系统疾病、肿瘤、脓毒血症等的治疗提供新途径。
中科院上海药物研究所周兵、唐炜、许叶春研究团队,以处于临床Ⅱ期的RIPK1变构抑制剂GSK2982772为起始,并根据该小分子与靶蛋白中的结合模式特点,开展基于结构的合理药物设计,得到一类作用于双口袋的高活性、高选择性的RIPK1抑制剂。2021年12月16日,相关研究工作以“Potent and Selective RIPK1 Inhibitors Targeting Dual-Pockets for the Treatment of Systemic Inflammatory Response Syndrome and Sepsis”为题,在线发表于Angew. Chem. Int. Ed。
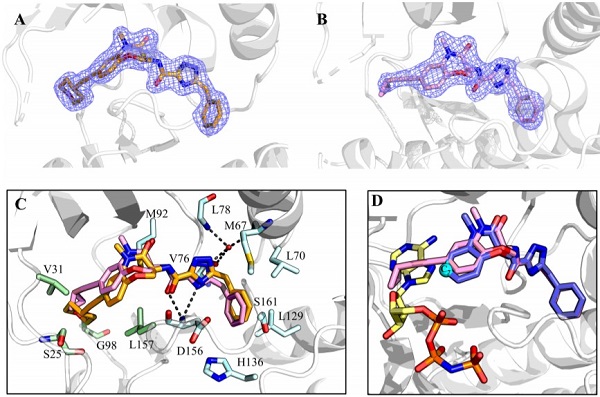
在TNFα诱导的U937细胞坏死模型中,该类衍生物相比较于阳性GSK2982772,抑制活性均提升10倍以上, IC50值达0.5 nM以下。进一步的晶体学研究表明,20/21号化合物同时占据了变构口袋以及ATP结合口袋,合理解释了抑制活性的提升。
在激酶谱的测试中,在1μM的测试浓度下,21号化合物表现出优异的激酶选择性。在小鼠药代动力学研究中,该化合物表现出良好的药代动力学性质,口服生物利用度>99%。在TNFα诱导的全身性炎症反应模型(SIRS)中,该化合物在保护小鼠体温方面显著优于阳性参考GSK2982772。在LPS诱导的脓毒血症模型中,21号化合物在恢复小鼠体温、存活率以及抑制小鼠体内细胞因子风暴等方面展现出明显优于阳性的药效。
综上,该研究揭示一类具有新颖作用模式的高活性、高选择性RIPK1抑制剂,有望为全身炎症性疾病、神经系统疾病等的治疗提供新策略。
上海药物所博士研究生杨向波、路慧敏以及上海药物所-南京中医药大学联合培养博士研究生谢航为文章的第一作者,周兵研究员、唐炜研究员以及苏海霞副研究员为本文的共同通讯作者。
该工作得到了国家自然科学基金、上海市科委等项目的资助。
图. 20/21号化合物结合模式分析
(供稿人:周兵/唐炜/许叶春课题组)